特集1 海外からの侵入を防ぐ
アフリカ豚熱
African Swine Fever (ASF)
汚染地域からの国内侵入リスクが高まる。

ここが
ポイント!
アフリカ豚熱(以下、ASF)にはまだ有効なワクチンはなく、迅速な診断による摘発淘汰(殺処分)しかありません。
もし、アフリカ豚熱ウイルス(以下、ASFV)が国内に侵入すれば急速にASFVは広がり、養豚業に深刻な打撃を与えるでしょう。アフリカからユーラシア大陸、そして2018年には中国でアジア初の発生が報告され、ますます国内侵入のリスクが高まっています。
農研機構はASFVの生態や特性を明らかにし、世界で初となるワクチン開発に挑むことで日本だけではなく世界の動物衛生に貢献します。

アフリカ豚熱とは
アフリカ豚熱(ASF)はアフリカ豚熱ウイルス(ASFV)の感染によって起こる豚とイノシシの伝染病で、症状が豚熱(CSF)に似ていますが、全く別の病気です。急性型のASFでは、感染後1週間程度で発熱、食欲不振などの症状が現れ、その致死率は100%に達します。家畜の監視伝染病に指定されています。ASFVは感染力が非常に強い上に、自然環境下での抵抗性も高く、感染豚を材料とした非加熱ソーセージなどの加工品の中で数日から数カ月間も感染力を保持できます。
画期的なIPKM細胞の開発により、世界初のASFワクチン開発に弾み

動物衛生研究部門
越境性家畜感染症研究領域 海外病グループ
上級研究員舛甚 賢太郎
MASUJIN Kentaro
横のつながりが生んだ成果
2021年3月に、「アフリカ豚熱ウイルスが効率よく増殖できる豚由来の細胞株を開発」※1という研究成果を発表しました。この成果は、農研機構内の生物機能利用研究部門(以下、生物研)と動物衛生研究部門(以下、動衛研)のコラボで生まれたもので、農研機構内の横のつながりで生まれた成功例だと思います。生物研の竹之内さん※2と動衛研の私は、私がBSE※3の研究に関わっていた時に一緒に仕事をした仲で、その後も互いに情報をやり取りできる関係でした。当時、竹之内さんは、樹立に成功した豚由来の細胞株(IPKM細胞)の新たな利用法を探しており、私はASFVに感染する優れた細胞株を探していました。竹之内さんからIPKM細胞を紹介されたその瞬間、「IPKM細胞は、もしかしたらASFの研究に使えるかもしれない」とお互いの要求と思いが一致したことが始まりです。いまでもこの偶然に感謝しています。
【注釈】
※1 : (研究成果)アフリカ豚熱ウイルスが効率よく増殖できる豚由来の細胞株を開発
※2 : 生物機能利用研究部門 生物素材開発研究領域 動物モデル開発グループ 主席研究員 竹之内 敬人
※3 : 牛海綿状脳症。牛の病気の一つで、BSEプリオンと呼ばれる病原体に牛が感染した場合、牛の脳の組織がスポンジ状になり、異常行動、 運動失調などを示し、死亡する
ASF克服の最前線の研究IPKM細胞

ASFVの基礎研究やワクチン開発を目指す中で研究の進展を妨げる大きな要因の一つが、ASFVを効率的に増殖させることが難しかったことです。ASFVは豚やイノシシのマクロファージ1)や単球に感染して複製するため、ASFVの増殖には、これらの動物から採取した新鮮な細胞(初代細胞2))が利用されるのですが、これらの細胞は試験管内で増殖しないため、手に入れられる細胞数に限界があること、手に入れた細胞の生存率や品質にばらつきがあること、また採取用の動物が予想外に病原体に感染している可能性を否定できないことなどから、安定的に多量のウイルスを得ることができませんでした。しかしIPKM細胞では非常に効率よくASFVを増やすことができます。また、IPKM細胞は不死化細胞3)なので、シャーレの中でどんどん増やすことができますし品質にばらつきがありません。いつも同じ状態で多くの実験ができることは研究を進める上でとても重要なことです。これらのことから、IPKM細胞は初代細胞よりも研究をする上で非常に有益な細胞であり、労力やコストの削減、アニマルウェルフェアなどにも貢献できます。
ASFVの起源や生態は未だ多くの謎に包まれていて、ワクチンなど有効な予防法や治療法も今は確立されていません。IPKM細胞を使った研究ができることは、僕たちにとって最大の強みとなっています。このIPKM細胞で研究を進展させ、基礎研究やワクチン開発に貢献していきたいと考えています。ASFの克服に向けて、チャレンジは始まったばかりです。
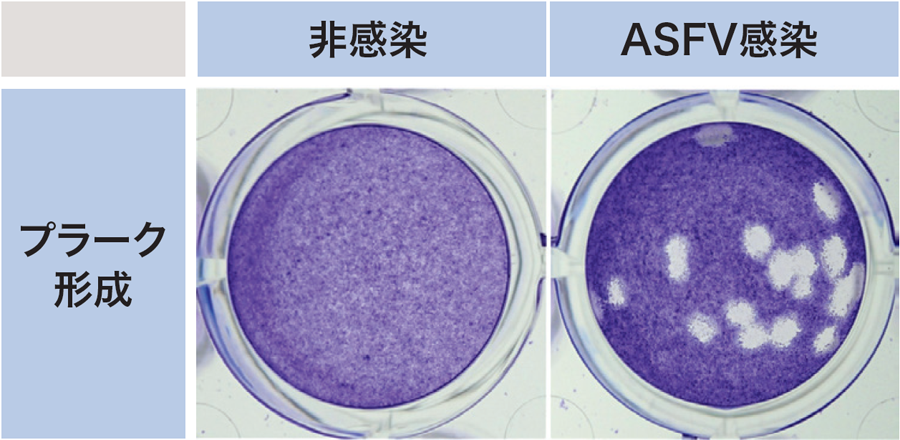
ASFV感染IPKM細胞株におけるプラーク形成
感染した細胞が変性、剥離して、プラーク(白色、円形の部分)が形成される
【用語解説】
1) マクロファージ : 白血球の1種。体内に侵入した異物を捕食して分解する役割を果たす
2) 初代培養 : 生体組織から直接採取して培養した細胞
3) 不死化細胞 : 無限に増殖する能力をもった細胞株

動物衛生研究部門
越境性家畜感染症研究領域 海外病グループ
北村 知也 研究員
KITAMURA Tomoya
ASFワクチン開発に挑む

ASFワクチン開発をターゲットとして研究をしています。国内ではまだ感染例はありませんが、2018年には中国でアジア初の感染が確認され、現在(2021年8月時点)ではアジアカ国まで拡大し、国内侵入のリスクが増大しています。仮に国内で発生したら、治療薬もワクチンもありませんので、摘発淘汰と周囲を含めた消毒が今できる対策です。
僕の研究では、様々な手法を用いて弱毒化したASFVを作出することで、弱毒化生ワクチンの開発を試みています。ASFVは、ゲノムの中に大体150から170ぐらいの遺伝子を持っているのですが、ある遺伝子を壊してみて、ASFVが弱毒化するかどうかを研究しています。この弱毒化ウイルスの作出は単純作業の連続に見えますが、確実にターゲットの遺伝子が壊れたウイルスを探し出すのも、そのウイルスを豚に感染させて弱毒化を確認するのも、時間や労力、十分な設備や実験資材が必要で、実は大変です。
しかし、IPKM細胞のようにASFVを効率良く増殖する細胞ができたことで、弱毒化ASFVの分離が大幅に楽になって、実験の効率が飛躍的に上がっています。少しでも早くワクチンを完成させたいと思っています。
世界初のASFワクチン開発への意気込み
未だ誰も有効なASFワクチンを作出できていないわけですから、日本だけではなく世界的に動物衛生に貢献できるので、非常にやりがいのある研究だと思います。
ASFでは、ASFVの遺伝子型にバリエーションがあり、少なくとも24種の遺伝子型があることがわかっています。わかりやすく言うと、新型コロナウイルスでアルファ株とかデルタ株などがあることと似ていて、遺伝子に多様性があります。例えば最近アジアで流行っているのは、遺伝子型Ⅱ型です。遺伝子型Ⅱ型のウイルスを弱毒化させた弱毒生ワクチンでこの流行しているASF感染を防ぐのが、小さなゴールです。その先は、遺伝子型Ⅰ型やⅣ型など、いろんな遺伝子型のASFVをマルチに防げるような、まさに遺伝子型を超えてASFVを防ぐワクチンの創出を大きい目標としています。
研究室訪問

写真上段左から : 生澤充隆研究員、北村研究員、亀山健一郎主任研究員
写真下段左から : 渡邉瑞季さん(日生研からの招へい研究員)、舛甚上級研究員
