研究項目及び実施体制(◎は研究代表者)
- 昆虫成長因子の作用機構解明と新規成長因子の探索(研究代表者:
(◎早川洋一/北海道大学低温科学研究所) - ヒト細胞に活性を示す昆虫成長因子の構造改変と新薬開発
(河野敬一/富山医科薬科大学薬学部) - 昆虫成長因子の機能と情報伝達の解明
(神村 学/独立行政法人農業生物資源研究所)
研究の目的
哺乳類ではこれまで数多くの細胞成長因子が発見され、各方面への応用研究も進んでいる。一方、昆虫においては、その報告例も少なく、これまで集中的かつ体系的に推進されたことのない未知なる研究分野と言える。本研究の目的は、昆虫細胞成長因子の概括的理解を目標に、その利用も視野に入れた基礎研究を行うことにある。
研究の内容
昆虫から同定されたペプチド性細胞成長因子第1号であるGBP(growth-blocking peptide)をモデルペプチドとしてその多角的基礎研究、さらに、新規細胞成長因子の探索を2つの主要課題に据えて研究を行った。その結果、GBPの各種多機能性を実証することができ、さらに、その多機能性の要因について考察を深めることができた。また、複数の新規細胞成長因子を同定し、その幾つかの因子については一次構造の決定に成功した。
主要な成果
- GBPは、細胞増殖作用の他に、幼虫発育調節、麻痺誘起作用、血球活性化作用といった多機能性を示し、特に、細胞増殖作用と血球活性化作用を示すGBP最小構造が異なることを明らかにした。
- GBPレセプター解析の結果、血球細胞のGBPレセプターは解離定数Kdが1~3nMの中親和性一種類であるのに対して、昆虫培養細胞High FiveのKd値は0.26nMと13.7nMの高親和性、低親和性の二種類が存在することを見い出した。
- GBPは胚発生の過程で、生理機能が未知とされてきた食道下体と言われる組織から分泌され、左右一対の頭原基を成長過程で中央に寄せて融合させる作用を担っていること突き止めた。
- 昆虫血球細胞の一種であるエノシトイドは、GBPによって細胞崩壊し、その過程でGBPに特異的結合性を示すGBP結合タンパク質を放出することを発見した。その一次構造を決定し、新規のタンパク質であることを証明した。
- 複数種の昆虫のGBP遺伝子構造を解析し、GBPコーディング領域の上流に2種類のORFが存在することを明らかにすると共に、これらが真核生物では非常に珍しいポリシストロニックな翻訳調節を受けている可能性を見い出した。
- これまで鱗翅目昆虫のみからしか見つかっていなかったGBPであるが、ヒツジギンバエからGBP様活性を持つペプチドを単離し一次構造決定に成功した。このペプチド構造を基に、ショウジョウバエとカのデーターベースから各々複数種の類似ペプチドが同定でき、GBP様低分子ペプチド族の昆虫類における普遍的存在の可能性を示した。
- BmPP(カイコGBP)の形質転換カイコ作成に成功し、強制発現によって幼虫発育が著しく遅れることを見い出した。
見込まれる波及効果
遺伝子工学的実験手法の確立によって、貴重な微量生理活性タンパク質の生産工場と称されるカイコであるが、その人為的な発育調節技術は必ずしも十分とは言えない。今回、形質転換カイコにおいて、GBP発現量を調節することによって、その幼虫発育速度を操作することが可能であることが明らかにした。従って、今後、さらに正確にGBP発現量を調節し得る形質転換体を作成することによって、より有用な昆虫工場としてのカイコの供給が可能になるものと期待できる。
主な発表論文
- Matsumoto Y., et al.: Insect cytokine, Growth-blocking peptide, triggers off a termination system of cellular immunity by inducing its binding protein: J. Biol. Chem., 278: 38579-38585 (2003)
- Tada M., et al.: Role of aromatic residues in the structure and biological activity of the small cytokine, growth-blocking peptide (GBP): J. Biol. Chem., 278: 10778-10783(2003)
- Aizawa T., et al.: Structure and activity of the insect cytokine growth-blocking peptide: J. Biol. Chem., 276: 31813 ? 31818 (2001)
- Ohnishi A., et al.: Characterization of receptors of insect cytokine, growth-blocking peptide, in human keratinocyte and insect Sf9 cells: J. Biol. Chem., 276: 37974-37979 (2001)
- Kamimura M., et al.: Molecular cloning of silkworm paralytic peptide and its developmental regulation: Biochem. Biophys: Res. Commun., 286: 67-73 (2001)
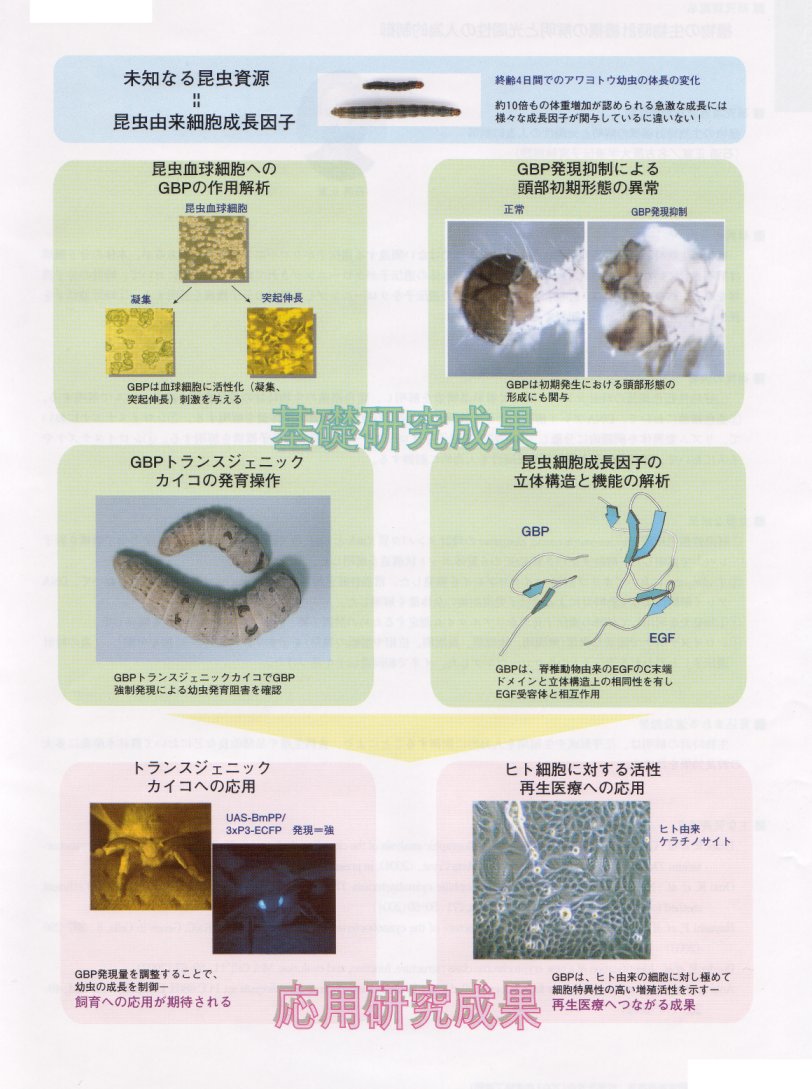
研究のイメージ