研究項目及び実施体制(◎は研究代表者)
- 「スーパープロテイン」の創出にむけた機能タンパク質の無細胞系新規選択法の開発と有用タンパク質の創生
(◎多比良和誠/東京大学大学院工学系研究科) - ラショナル・プロテイン・セレクション法による新機能糖結合タンパク質の創出
(長谷川典巳/山形大学・理学部) - 「スーパープロテインの創出にむけたタンパク質分子のデザインと構造解析」
(小林秀行/食品総合研究所)
研究の目的
機能性タンパク質とその遺伝情報とを1対1で結合させる機能を有する機能性リボ核酸を分子設計し、それを用いて無細胞系で新規機能性タンパク質を選択する新規の機能性タンパク質選択システムを開発する。また、これら技術の確立と同時に、構造機能解析、計算化学を駆使した分子デザイン、および非天然型アミノ酸側鎖の導入システムとの融合を行い、最終的には天然型を凌駕するスーパープロテインを創生する。
本課題では特に糖質分解酵素に注目し、単なる酵素の高機能化、高活性化だけにとどまらず、酵素反応のスイッチングが自由自在にできる酵素(スイッチングエンザイム)の創出にも着手する。
研究の内容
- 実際に応用が困難であった従来法よりも簡便に機能性タンパク質を選択できるシステムの開発を行った。
- これまで導入が困難であった非天然アミノ酸をタンパク質に導入するための手法の開発を行った。
- ラショナル・プロテイン・セレクションおよびデザイン法を用い、糖分解酵素の高機能化、高活性化を行った。
主要な成果
- 4種類以上の新規の機能性タンパク質選択システムを独自に開発した。これらの手法はターゲットの選択条件などに合わせた使い分けが可能であり、酵素などを活性で選択することが可能な手法を含む。さらに、これら手法を用いて従来法よりもより強くリガンドに結合する新規ペプチドを創出した。
- アジ化ナトリウムで活性を自由自在にスイッチでき、しかも反応過程で生成物(天然にない修飾糖)と未反応物を分離できるスーパーキシラナーゼを創出した。またこの酵素の特長を生かし、そのX線結晶解析からキシラナーゼの酵素反応の全行程を世界で初めて可視化した。さらに、その構造情報を基に非天然アミノ酸の導入を加味した分子デザインにより、天然アミノ酸置換では不可能であった活性向上型キシラナーゼを創出した。
- 構造機能相関を調べることでキシラナーゼの基質特異性発現のメカニズムを解明した。また、ラショナル・プロテイン・デザイン法により2重の変位を導入することで酵素の基質特異性の制御を可能にした。
- 4塩基コドン法による非天然アミノ酸導入により、これまでにない蛍光波長を持つGFPを創出した。
見込まれる波及効果
- 我々の開発したラショナル・プロテイン・セレクション法を用いることで、従来作成が困難であった新規の高機能ペプチドの創出が容易となった。これは産業に対する経済的な効果は大きい。
- スイッチングエンザイム創出法は多くの糖質加水分解酵素で普遍な手法である。本酵素の特長である酵素反応の自在性、および新規修飾糖の生産能力は、新規産業への発展を大きく期待させるものである。
- スイッチングエンザイムは反応産物を一時的に保持することにより精製も容易であり、産業に対する経済的効果だけでも絶大なものと予想できる。
- 糖質加水分解酵素の高機能化や、基質特異性の制御を可能にしたことは食品産業、農林水産業等に対し有用な情報である。
主な発表論文
- Fujita S., et al. Novel approach for linking genotype to phenotype in vitro by exploiting an extremely strong interaction between RNA and protein. J. Med. Chem. 45 : 1598-606 (2002).
- Kaneko S., et al. Structure and function of a family 10 b-xylanase chimera of Streptomyces olivaceoviridis E-86 FXYN andCellulomonas fimi Cex. J. Biol. Chem. 279 : 26619-26626 (2004).
- Ito S., et al. Rational affinity purification of native Streptomyces family 10 xylanase. J. Biotechnol. 110 : 137-142 (2004).
- Sawata S.Y., et al. A system based on specific protein-RNA interactions for analysis of target protein-protein interactions in vitro. successful selection of membrane-bound Bak-Bcl-xL proteins in vitro. Protein Eng. Des. Sel. 17 : 501-508 (2004).
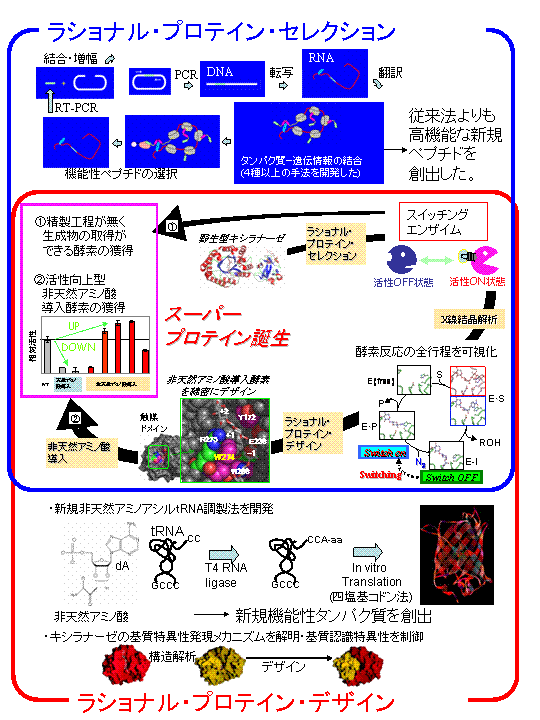
研究のイメージ