研究の目的
高齢社会を迎えた日本において、生活習慣病の増加は避けることのできない状況にあり、食品の機能を効率的に活用してこれを抑制することは緊急性を要しており,社会的要請度も高い。生活習慣病の発症に関わる多くの機能タンパク質(トランスポーター、転写因子、ホルモン受容体等)は、生体内のレギュレーター脂質により活性制御を受けている。これらの分子連関を統合的な研究体制のもと解明する。さらに食品成分の中にレギュレーター脂質活性を見出し、これらを高機能性食品として活用する試みにより、新技術・新分野創出を目指す。
研究項目及び実施体制(◎は研究代表者)
- 転写因子、核内受容体による脂質代謝制御機構の解明とレギュレーター脂質による調節
(◎佐藤隆一郎/東京大学大学院農学生命科学研究科) - 脂質トランスポーターの活性調節機構の解明と高機能性食品による調節
(植田和光/京都大学大学院農学研究科) - 核内受容体を利用した骨増強食品素材評価系の構築に関する研究
(加藤茂明/東京大学分子細胞生物学研究所)
研究の内容及び主要成果
- コレステロール代謝を制御する転写因子SREBPと核内受容体とのタンパク質—タンパク質相互作用を介したクロストークについて新たな知見を得た。さらに,核内受容体活性を介して脂質代謝改善効果を発揮する分子メカニズムを明らかにした上で,受容体リガンド活性を有するレギュレーター脂質を食品成分から探索する評価系を駆使し,新たな機能を有するフラボノイドを複数見出した。
- ABCA1とABCG1の機能を明らかにし、食物性脂質メディエーターによる調節の基盤を築いた。特に、ABCA1を世界で始めて精製し、生化学的に解析することに成功した。さらにABCA1の新規な翻訳後活性調節機構を発見した。ABCG1のコレステロール輸送機構も明らかにした。
- 女性ホルモン欠乏は、重篤な骨減少を引き起こすことから、女性ホルモン受容体の骨組織での機能をノックアウトマウスを作製することで探り、女性ホルモン受容体(ERα)が破骨細胞で機能し、細胞死を誘導することで、女性ホルモンの骨防御作用を発揮することを見出した。また、骨形成を担う骨芽細胞の分化に核内受容体PPARγの機能抑制が生理的に重要であることを分子レベルで証明した。
見込まれる波及効果
食品成分からレギュレーター脂質を見出し、その機能を明らかにしたことにより,高機能性食品創製の可能性を提示することに成功した。さらに,同様な試みを介して異なる効果を有する食品創製を目指すことにより、新分野創出の波及効果が期待される。
主な発表論文
- Kanayama T., et al.: Interaction between Sterol Regulatory Element-binding Proteins and Liver Receptor Homolog-1 Reciprocally Suppresses Their Transcriptional Activities. J. Biol. Chem. 282: 10290-10298(2007)
- Nakahara M., et al.: Ileal bile acid-binding protein functionally associated with the farnesoid x receptor or ileal bile acid transporter regulates bile acid activity in the small intestine. J. Biol. Chem. 280: 42283-42289(2005)
- Nagao K., et al.: Enhanced apoA-I-dependent cholesterol efflux by ABCA1 fromsphingomyelin-deficient CHO cells. J. Biol. Chem. 282:14868-14874 (2007)
- Takahashi K., et al.: Purification and ATPase Activity of Human ABCA1. J. Biol. Chem. 281: 10760-10768 (2006)
- Nakamura T., et al.: Estrogen prevents bone loss via estrogen receptor a?and induction of Fas ligand in osteoclasts. Cell 130: 811-823 (2007)
- Takada I., et al.: A histone lysine methyltransferase activated by non-canonical Wnt signaling suppresses PPAR-g transactivation. Nat. Cell Biol. 9: 1273-1285 (2007)
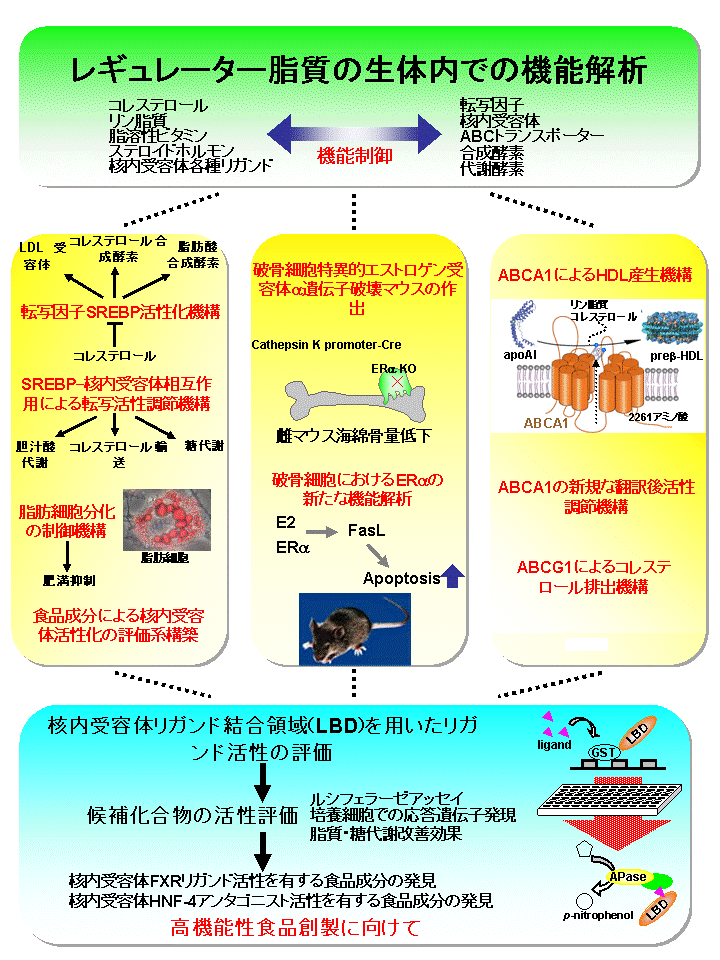
研究のイメージ