動物衛生研究部門
III.原子吸光法による飼料中 銅、亜鉛の測定
測定原理
飼料中の金属を測定するためには試料に強酸を加え加熱灰化する。その後灰化液を適当な濃度に希釈し原子吸光分光光度計で測定する
参考文献
- 衛生試験法・注解:日本薬学会編, 1990 金原出版
- 栄養診断のための栽培植物分析測定法:作物分析法委員会編, 1976 養賢堂
目次
1.準備物
(1)器具
- 原子吸光分光光度計(フレーム型)
- ケルダール分解装置
- ケルダールフラスコ (50 ml容) 30 ml容でも可
- 蒸発皿 (外径60 mm、平底) るつぼでも可
- 試験管バサミ、るつぼバサミ
ガラス器具は酸洗浄済みのもの
-酸洗浄-
通常の洗浄は、1%硝酸に一晩浸けて乾燥させる
原子吸光分光光度計(定量演算機能付き)

ケルダール分解装置(水流ポンプ付き) 

ケルダールフラスコ(50ml容)、蒸発皿、試験管バサミ、るつぼバサミ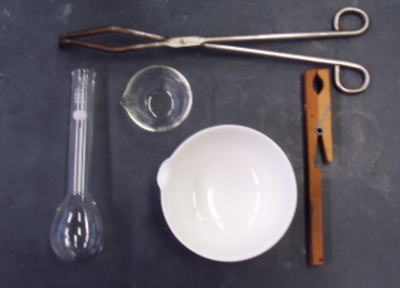
(2)試薬
- 硝酸 (精密分析用)
- 硫酸 (精密分析用)
- 過塩素酸 (精密分析用)
- 塩酸 (精密分析用)
- 銅、亜鉛標準液 (原子吸光分析用)
2.試薬調製法 (原子吸光法による臓器中 銅、亜鉛の測定と同様)
(1)標準液
銅、亜鉛二種混合高濃度標準液
メスフラスコに銅標準液 1.0 ml、亜鉛標準液 0.5 mlを入れ、1N 塩酸を加え全量を100 mlにする(表-1)
(表-1)
| 市販品 | 標準液 | 1N塩酸 | 濃度 |
|---|---|---|---|
| 銅標準液 (1000 mg/L) |
1.0 ml | 全量を100 mlにする | 銅濃度は1000 μg/dl 亜鉛濃度は500 μg/dl |
| 亜鉛標準液 (1000 mg/L) |
0.5 ml |
銅、亜鉛二種混合測定用標準液
高濃度標準液を所定量取り、1N 塩酸で全量を10 mlにする(表-2)
(表-2)
| 標準液 | 高濃度標準液 (ml) |
1N 塩酸 (ml) |
全量 (ml) |
最終銅濃度 (μg/dl) |
最終亜鉛濃度 (μg/dl) |
| Blank | 0.00 | 10.0 | 10.0 | 0 | 0.0 |
| Std 1 | 0.25 | 9.75 | 10.0 | 25 | 12.5 |
| Std 2 | 0.50 | 9.5 | 10.0 | 50 | 25.0 |
| Std 3 | 1.00 | 9.0 | 10.0 | 100 | 50.0 |
| Std 4 | 2.00 | 8.0 | 10.0 | 200 | 100.0 |
(2)試薬
- 過塩素酸:硫酸(4:1)混液
作製する混合液の倍以上のビーカーに、過塩素酸を静かに入れる。
次いで、ガラス棒を伝わせ硫酸を少量ずつ加える
100 mlの混合液を作る場合は200~300 mlのビーカーを使用
混合液は発熱するので注意 - 1N 塩酸および6N 塩酸
濃塩酸を蒸留水で12倍および2倍する。
酸塩基試薬調整法
3.操作手順
(1)飼料の乾燥
- 飼料を入れる容器(12 cmの蒸発皿)を105 °C、3時間乾燥後、デシケータ内で30分以上冷ます。その後、重量を測定し恒量を求める。
- 粗飼料は(生草、乾草)を10 mm位にハサミでカット、ペレット状の濃厚飼料はミキサーで粉砕する。(ミキサーは電動コーヒーミルが便利)
- 恒量を求めた蒸発皿に試料を入れ重量を測定する
- 試料の入った蒸発皿を105 °Cで3 時間乾燥後、デシケータ内で30分以上冷ます。その後、重量を測定し飼料中の水分含量を求める
(2)サンプル秤量
- 空のケルダールフラスコを電子天秤にのせ、ゼロ調節をする。
- 乾燥したサンプル約2 gを フラスコに入れる。
- サンプルを入れたフラスコを天秤に載せて秤量、サンプル量を記録。
試料はやや大きめが良い。細かくしすぎると突沸の原因となる。
粗飼料を10 mmぐらいにカット
ペレット状の濃厚飼料をミキサーで粉砕(前)
ペレット状の濃厚飼料をミキサーで粉砕(後)
フラスコに試料を入れる 左:濃厚飼料 右:乾草
(3)硝酸20 mlを加え、ラップをかけてドラフト内に一晩放置。
硝酸添加後、一晩置くと良く分解され、突沸しにくい。
硝酸の量はケルダールフラスコ容量の1/2以下にする。
粉末状の試料(配合飼料等)の場合、硝酸を入れた後にフラスコを振らないこと。
多量の泡が発生し、サンプルがあふれ出ることがある。
硝酸添加直後
硝酸添加10分後
硝酸添加30分後 右側:小さな泡が出る
硝酸添加一晩放置後 左側も泡が出ている
(4)ケルダール分解装置で加熱分解。
- 初めは低い温度(少量の泡が出て、褐色の発煙がある程度)で行なう。
分解初期には小さな泡が出る、分解が進むと大きな泡になり、さらに進むと泡は出なくなる - 泡の出が少なくなってきたら徐々に温度を上げる。
ケルダールフラスコの先端部分が熱くなる
先端部分が熱くならない時には装置の温度を上げるか、アルミ箔で首の部分を包み、強く加熱しない。
突沸しそうな時は装置から外して少しさます。
1時間後、液量が10 ml位になったら、装置からおろして放冷する。
粗飼料は硝酸では分解されない物が多い、液量が少なくなると突沸の危険が増すので早めに終了する
分解開始 左:濃厚飼料 右:乾草
分解開始5分後、小さな泡が盛んに出ている
分解開始15分後 左は大きな泡に変化する
ケルダールフラスコの首の部分をアルミ箔で包む
アルミ箔で包んだときの試料右側は繊維状の物で白く見える
分解開始30分後褐色ガスの色も薄くなる
分解開始1時間後さらに色も薄くなり液量も減る
硝酸分解終了
(5)過塩素酸:硫酸(4:1)混液を10 ml加え再びケルダール分解装置で加熱分解。
加温は、まず低温で分解、その後1時間ほどかけて高温まで徐々にあげてゆく。
2~3時間後、泡が出なくなり、液量が2~3 ml、無色から薄い黄色、透明になれば分解終了、放冷する。
このステップでは加熱分解中に過塩素酸が蒸発し、硫酸が残る。
過塩素酸-硫酸混液で分解開始
分解開始10分後液が温まると褐色ガスが出る
分解開始15分後褐色ガスの出が多い
分解開始30分後褐色ガスの出が弱まる
分解開始1時間後色が薄くなる
分解開始2時間後液量が少なくなる
分解開始3時間後泡が出なくなり白煙が出る
過塩素酸-硫酸混液分解終了(無色不透明)
(6)灰化液を蒸発皿に移す
- フラスコ内に蒸留水を3 ml加え灰化液と混合する(発熱注意)
- 混合液を蒸発皿に移す。
- フラスコに再度蒸留水3 mlを入れ共洗いし、蒸発皿に加える、この操作をもう一度繰り返す。
白く見えるものは不溶性物質(ケイ酸)
(7)蒸発皿をケルダール分解装置上で加熱し溶媒を蒸発させる。
- 蒸発皿の上部(20 cm位)にアルミ箔でゴミよけのおおいをし、加熱する。
- 完全に蒸発する直前に装置から降ろして放冷。
乾固すると測定成分が失われることがあるので注意!!
(8) 6N 塩酸で再溶解
- 蒸発皿に6N 塩酸 10 ml入れ試料を再溶解する。
- パスツールピペットを用い蒸発皿内部をよく洗い試料を溶解する。
- 100 mlのメスシリンダーに再胃液を溶解液を入れる。
- 蒸留水で蒸発皿を共洗いし、洗液をメスシリンダーに加える(2回洗う)。
- 蒸留水を加え全量を60 mlにする(塩酸の終末濃度は1Nになる)。
- 不溶性物質を遠心して除く(2,000回転 5分間)
(9)原子吸光装置で測定。
- 銅は324.8 nm、亜鉛は213.9 nmの吸収波長を測定する。
- 銅は(8)で作成した液をそのまま測定する。
- 亜鉛は(8)で作成した液を2倍希釈し測定する(希釈液は1N 塩酸)
灰化液とフラスコを共洗いした液を蒸発皿(るつぼ可)に入れる
上部にアルミ箔でゴミよけの覆いをし、蒸発開始
加熱すると白煙が出る
左側は蒸発終了 右側は液が残っている
灰化液の蒸発終了
6N 塩酸で再溶解、蒸留水で共洗いし全量を60 mlにする
左:遠心分離前は白濁 右:遠心分離後は透明
原子吸光装置で測定
4.補足説明
(1)検量線
標準溶液から検量線を作成する
定量演算機能が付いていれば機械が作成する、サンプルを測定すると自動的に濃度が計算されプリントアウトされる
(2)計算
検量線から得られたデータを下記の式に当てはめれば飼料中の銅、亜鉛の量が求められる
a×(b/c)÷d = μg/g
a :検量線から得られたデータ(μg)
b :再溶解液量(銅は60 ml、亜鉛は120 ml)
c :標準液量(銅、亜鉛とも100 ml)
d :試料量(乾物重量 g)
(3)正常値(当研究所調べ)
イネ科牧草
- 銅 6~10 μg/g
- 亜鉛 20~50 μg/g
(4)参考資料
日本標準飼料成分表(2001年版), 中央畜産会

