迅速かつ高精度なASF(アフリカ豚熱)遺伝子検査法の開発
要約
開発した遺伝子検査法は、制限酵素認識配列を導入した陽性対照試料を使用することで、陽性対照試料の交差汚染による誤判定を防ぐことが可能となり、ASFを迅速かつ高精度に判定できる。本法は国の防疫指針に基づいて都道府県が実施する病性鑑定の検査法として採用され、豚およびイノシシのASF遺伝子検査法に利用される。
- キーワード:ASF、遺伝子検査、コンベンショナルPCR、病性鑑定、防疫指針
- 担当:動物衛生研究部門・越境性感染症研究領域・アフリカ豚熱ユニット
- 代表連絡先:電話 029-838-7895
- 分類:普及成果情報
背景・ねらい
2007年に欧州に侵入し、2018年にはアジアで初めて発生したASFは現在も近隣のアジア諸国で猛威を振るっている。罹患豚のほぼ100%が死に至るほど病原性の強い本病に対しては未だに有効な予防法、治療法が開発されておらず、バイオセキュリティーの強化と迅速なウイルスの検知のみが有効なまん延防止対策となっている。また、2018年4月には空港で収去された豚肉加工品からASFウイルス(ASFV)が分離されたほか、同年9月以降は国内で類症疾病であるCSF(豚熱)が続発していることから、簡便で迅速なASF特異的検査法の開発が求められている。コンベンショナルPCR法は、簡便で迅速な遺伝子診断法として広く普及しているが、陽性対照試料の検査材料への汚染による誤判定の危険性が常に存在する。そこで、本研究では、都道府県家畜保健衛生所等での検査に利用可能で交差汚染による誤判定を防ぐための陽性対照試料を新たに合成し、これを用いて迅速かつ高精度なASFのPCR検査法を開発する。
成果の内容・特徴
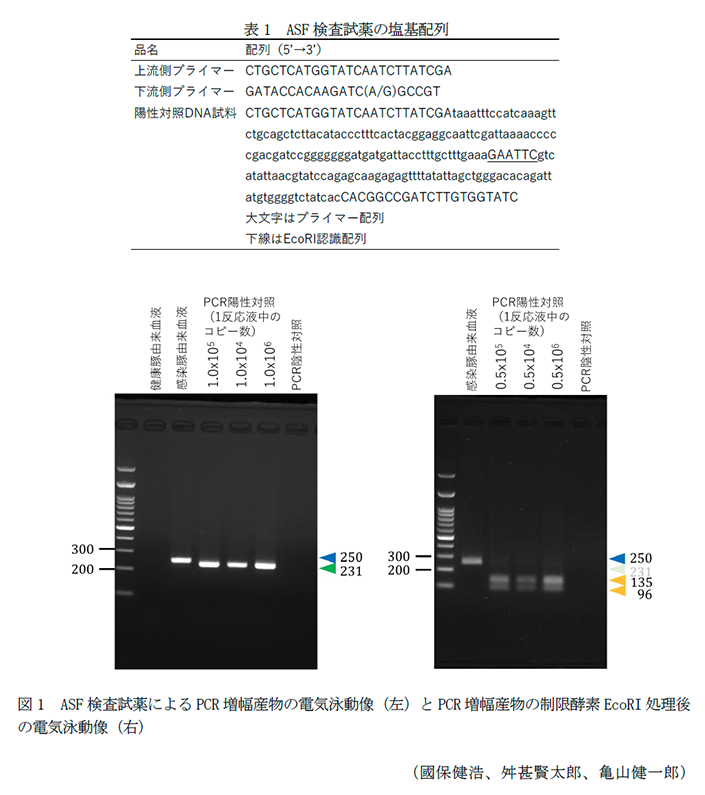
- OIEマニュアルを参考にしてASFV に特異的なゲノム配列の上流側および下流側にプライマーを設計する。また、これらのプライマーで増幅可能でASFVには存在しない制限酵素認識配列を人為的に挿入したDNA試料を陽性対照用試料として作製する(表1)。
- 感染豚由来血液及び陽性対照試料を上記のプライマーを用いてPCR反応を行うと、感染豚由来血液からは250bp、陽性対照試料からは231bpの増幅産物が得られる(図1左)。
- 増幅産物を制限酵素EcoRIで消化すると、陽性対照試料由来増副産物からは135bpおよび96bpの断片が得られるのに対し、感染豚由来血液由来増幅産物は切断されないことから、実際の感染に基づく増幅と陽性対照試料の混入による増幅を区別することができる(図1右)。
普及のための参考情報
- 普及対象:都道府県家畜保健衛生所、動物検疫所、動物医薬品検査所等
- 普及予定地域・普及予定面積・普及台数等:プライマー、陽性対照試料およびマニュアルからなる検査キット(60,000検体分)を上記機関54か所に配布済み。
- その他:本法は「アフリカ豚熱に関する特定家畜伝染病防疫指針」に収載されている。
具体的データ
その他
- 予算区分:交付金、その他外部資金(戦略的監視診断)
- 研究期間:2018年度
- 研究担当者:國保健浩、舛甚賢太郎、亀山健一郎、岡寺康太、北村知也
- 発表論文等:農林水産省(2019)「アフリカ豚熱に関する特定家畜伝染病防疫指針」(2019年10月15日公表)
