牛由来肝実質細胞株と肝類洞壁細胞株との共培養は薬物代謝酵素を相乗的に誘導する
要約
牛の肝臓から樹立した肝実質細胞株は、牛の肝類洞壁細胞株と共培養することによって、単独培養と比べて薬物代謝遺伝子発現が向上する。この共培養法は、薬物の牛に対する簡便な毒性評価に利用できる。
- キーワード:牛、肝実質細胞、肝類洞壁細胞、薬物代謝酵素、毒性評価法
- 担当:動物衛生研究部門・病態研究領域・中毒・毒性ユニット
- 代表連絡先:電話 029-838-7895
- 分類:研究成果情報
背景・ねらい
牛の代謝病や安全性の研究には、動物福祉および経済性の観点から、細胞を用いた動物実験代替法の開発が望まれるが、細胞株等では初代培養に比べて著しい肝機能の低下が知られており、個体や臓器と同様の薬物代謝や代謝応答、毒性を反映する細胞実験系は確立されていない。代謝の中心である肝臓には肝実質細胞に加えて、クッパー細胞、筋線維芽細胞、類洞内皮細胞等の肝類洞壁を構成する細胞が存在し、互いに協働して異物に対する生体防御を行っている。そこで、本研究では牛の肝臓から作出した肝実質細胞株と肝類洞壁細胞株を組み合わせた共培養系を開発し、これらの細胞の相互作用による牛の薬物代謝関連遺伝子の発現動態を明らかにする。
成果の内容・特徴
- 牛の肝臓から樹立した肝実質細胞株(BH4、BH5)のそれぞれに対して、同じく牛肝臓から樹立した筋線維芽細胞株(A26細胞)または類洞内皮細胞株(B46細胞)を1:2の混合比になるようにコラーゲンコートしたプラスチックシャーレに播き、血清添加培地で48時間培養することで、シャーレ全体が細胞で覆われ、一定の細胞密度になる培養条件が確立される。
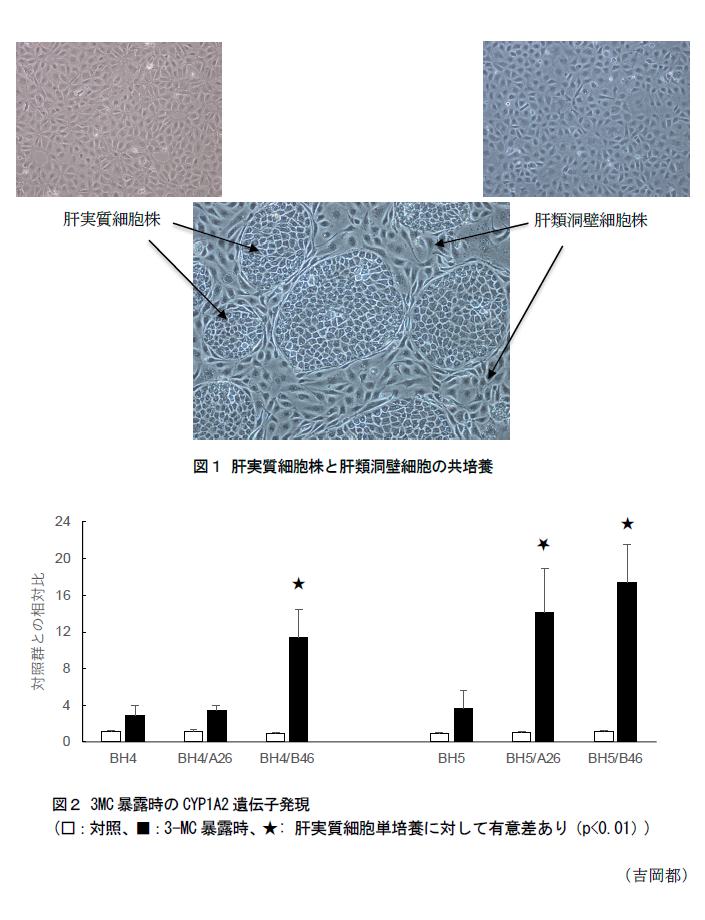
- 2種類の細胞を共培養すると、肝実質細胞株の周囲を肝類洞壁細胞が取り囲むような形態をとり、微小組織培養系が形成される(図1)。培養48時間後に牛初代培養肝細胞用に開発した無血清培地に交換することで、血清中の生理活性物質の影響を受けず、細胞から産生される代謝産物や生理活性物質の解析が可能な培養系ができる。この共培養系は、約1週間程度の維持培養が可能であり、化学物質の影響を評価する試験等に利用が可能である。
- 薬物代謝酵素誘導剤である3-メチルコラントレン(3-MC)を暴露すると、肝実質細胞株と肝類洞壁細胞株の共培養においては、肝実質細胞株の単培養時と比較して、薬物代謝酵素チトクロームP-450(CYP)のうちCYP1A1、CYP1A2およびCYP1遺伝子の発現が上昇する。とくに、BH4細胞とB46細胞、BH5細胞とA26またはB46細胞との組み合わせでは、肝臓特異的な薬物代謝酵素であるCYP1A2遺伝子の誘導が肝実質細胞単培養と比較して有意に上昇する(図2)。
成果の活用面・留意点
- 肝臓での解毒代謝の中心である肝実質細胞株と肝類洞壁細胞株の共培養は、牛の飼料由来有害物質の新しい動物実験代替法への応用が可能である。
- 牛由来肝実質細胞株と肝類洞壁細胞株の共培養は、薬物代謝以外の肝機能においても細胞間の協働による機能向上が期待できることから、牛の肝臓における毒性のほか、代謝病などの病態発現機序の解明に有用である。
具体的データ
その他
- 予算区分:交付金、競争的資金(科研費)
- 研究期間:2017~2019年度
- 研究担当者:吉岡都、竹之内敬人、木谷裕、グルゲ キールティ シリ、山中典子
- 発表論文等:Yoshioka M. et al. (2019) In Vitro Cellular & Development Biology-Animal, doi: 10.1007/s11626-019-00408-6.
