初代培養肝細胞を用いたダイオキシン型毒性物質のバイオアッセイ法
※アーカイブの成果情報は、発表されてから年数が経っており、情報が古くなっております。
同一分野の研究については、なるべく新しい情報を検索ください。
要約
牛および鶏の初代培養肝細胞とRT-PCR法および酵素活性測定を組み合わせた、ダイオキシン型毒性物質の高感度バイオアッセイ法を開発した。本法では、2,3,7,8-TCDDとして100fMのダイオキシン型毒性物質を検出可能である。
- キーワード:ダイオキシン、バイオアッセイ、初代培養肝細胞、シトクロムP-450
- 担当:動衛研・安全性研究部・毒性物質制御研究室
- 連絡先:電話029-838-7821
- 区分:動物衛生
- 分類:科学・参考
背景・ねらい
ダイオキシン類は、アリルハイドロカーボンレセプター(AhR)を介してシトクロムP-450(CYP)などの薬物代謝酵素遺伝子の発現を誘導してその毒性を発揮する。また、ダイオキシン類以外のいくつかの新規な残留性有機汚染物質も同様の機序で毒性を表すことが示唆されている。そこで、AhRを介して毒性を示す環境汚染化学物質の影響を評価する手段として、薬物代謝の主要な場である肝細胞の初代培養系を用いて、これらの遺伝子の発現を指標としてダイオキシン型毒性物質を高感度に検出するバイオアッセイ系を構築した。
成果の内容・特徴
- 肝特異機能が長期間持続し、特に薬物代謝酵素群の維持に優れた培養系の作出を検討した。牛肝細胞についてはスフェロイド培養法を、鶏肝細胞についてはiNOS合成阻害剤(L-NAME)添加培養法をそれぞれ確立した。
- 牛CYP1A1については我々が決定した部分塩基配列をもとに、その他の遺伝子は既知の配列をもとに、RT-PCR用プライマーを設計するとともに、RT-PCR反応条件を設定し、これらの遺伝子の発現を検出可能とした。
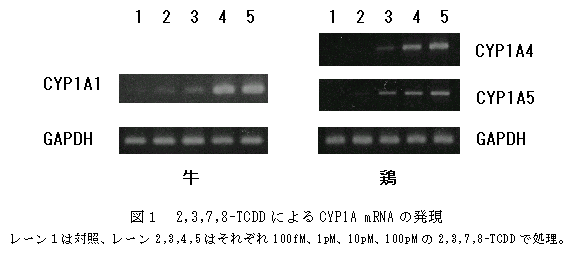
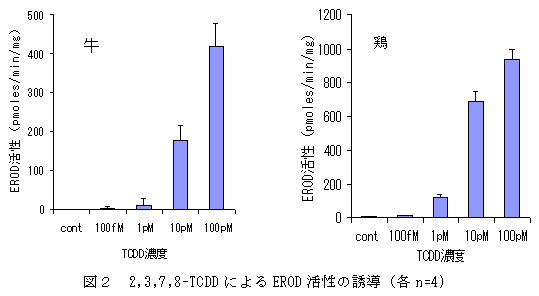
- この培養系にダイオキシン(2,3,7,8-TCDD)を24時間感作させ、CYP1A群遺伝子の発現を観察したところ、牛では100fMという低用量から、用量依存的にCYP1A1 mRNAの発現がみられた(図1)。鶏では1pMから用量依存的にCYP1A4および1A5 mRNAの発現が観察された(図1)。また、CYP1A群遺伝子産物のethoxyresorufin-O-deethylaseとしての活性(EROD活性)も、100fMから用量依存的に上昇していた(図2)。
- 培養細胞におけるダイオキシンによるCYP遺伝子の誘導について、100fMレベルでの影響は報告されておらず、本実験系の有用性が確認された。
成果の活用面・留意点
今回確立した実験系は、100fMというきわめて低濃度の2,3,7,8-TCDDの影響を検出できることが明らかになった。このバイオアッセイ系を用い ることにより、試料中に混在するAhRを介して毒性を示す物質(ダイオキシン型毒性物質)の総毒性を、2,3,7,8-TCDDに対する相対値として、高 感度に検出することが可能と考えられる。
具体的データ
その他
- 研究課題名:牛および鶏の肝機能に対する内分泌かく乱物質の影響の解明
- 予算区分:委託プロ(環境ホルモン)
- 研究期間:1999~2002年度
- 研究担当者:山中典子、グルゲ キールティー シリ、宮崎茂
- 発表論文等:1) Guruge et al. (2001) Organohalogen Compounds 53:251-254.
2) Yamanaka et al. (2001) Organohalogen Compounds 53:255-257.
