ポイント
- 2016年11月青森県及び新潟県で発生した高病原性鳥インフルエンザ1)の原因ウイルスの全ゲノム配列を解読しました。
- ゲノム配列から国内の野鳥由来のH5N6亜型2)ウイルスと同一の由来であると推定されました。
- これらのウイルスは中国で分離されたH5N6亜型ウイルスとその他の鳥インフルエンザウイルスとの遺伝子再集合3)ウイルスであることがわかりました。
- このウイルスが直接、人に感染する可能性は低いと推定されました。
概要
- 農研機構動物衛生研究部門では、11月28日に青森県および新潟県で発生した高病原性鳥インフルエンザ(Highly pathogenic avian influenza: HPAI)の原因ウイルスの亜型を同定すると共に、全ゲノム解析を行い遺伝子レベルでウイルスの由来や病原性の推定を行いました。
- 青森県および新潟県で発生したHPAIの原因ウイルス(青森株、新潟株)をH5N6亜型高病原性鳥インフルエンザウイルス(HPAIV)4)と同定するとともに、次世代シークエンサー5)を用いて、それぞれのウイルスゲノムの99.5%(青森株)および100%(新潟株)の塩基配列を決定しました。決定した2つのウイルスの塩基配列は、8本のRNA分節6)全てにおいて相互に99.2%以上の相同性を持ち、また鹿児島出水市のナベヅルのねぐらの水から分離したウイルスとも99.3%以上の相同性を示しました。
- 8本のRNA分節について、公共遺伝子データベースで公開されているインフルエンザウイルス遺伝子との比較を行ったところ、全ての分節において韓国で分離されたH5N6亜型HPAIV(韓国株)と97.4%以上の相同性を持つことが明らかとなりました。また、8本の遺伝子分節のうち7本の遺伝子分節は、2015年流行していたH5N6亜型HPAIVと、1本の遺伝子分節はその他の鳥インフルエンザウイルス(AIV)とそれぞれ97%以上の相同性を示しました。
※ただし、この結果は直接的なウイルスの由来を示すものではありません。 - 決定された塩基配列から推定されるアミノ酸配列をもとに、人への感染のリスクを評価しました。青森株及び新潟株には、これまでに報告されている人への感染性に関与すると考えられるアミノ酸変異は認められなかったことから、本ウイルスが直接、人に感染する可能性は低いと考えられます。
予算
農研機構運営費交付金、文部科学省「感染症研究国際ネットワーク推進プログラム」
背景
2014年から2015年にかけて日本国内において、H5N8亜型インフルエンザウイルスによるHPAIが発生し、家禽産業に甚大な影響を与えました。同時期に野鳥からも家禽のウイルスと類似したH5N8亜型HPAIウイルスが分離されています。また、アジアで流行したH5N8亜型HPAIウイルスはヨーロッパや北アメリカにも拡散し、北アメリカではウイルスの遺伝子再集合によりH5N2亜型ウイルスが出現して大規模なHPAIが発生しました。
H5N6亜型ウイルスに関しては、2013年以降中国でH5N6亜型ウイルスによるHPAIの発生が報告されたのを皮切りに、2016年秋以降に韓国でもHPAIの発生が報告されています。
国内では、2016年11月に鹿児島県出水市のナベヅルのねぐらの水からH5N6亜型ウイルスが分離されたのを初めとし、秋田県の動物園で死亡したコクチョウや鳥取県のカモ糞便、岩手県で死亡したオオハクチョウ等、各地で野鳥からH5N6亜型ウイルスが検出されています。
経緯
2016年11月28日に青森県青森市のあひる(フランス鴨)農場および新潟県関川村の採卵養鶏場でHPAIの発生が認められました。農研機構動物衛生研究部門では鳥インフルエンザの確定診断機関として、HPAI発生を引き起こしたA型インフルエンザウイルスの亜型同定、病原性試験を行うとともに、ウイルスの全ゲノムの解析を行いました。
内容・意義
- 青森家畜保健衛生所で採取された気管および総排泄腔スワブならびに新潟県中央家畜保健衛生所で分離されたA型インフルエンザウイルスから抽出したRNAを用いて、赤血球凝集素タンパク質(HA)とノイラミニダーゼ(NA)をコードする遺伝子の配列を決定し、H5N6亜型であることを確定しました。この亜型は今年の秋以降国内の野鳥などから分離されているHPAIVや韓国で発生しているHPAIの原因ウイルスと同じです。また、それぞれの農場で死亡したあひる、鶏から分離されたウイルス(青森株および新潟株)を国際獣疫事務局(OIE)の定める術式に従ってBSL-3ag7)動物実験室内で鶏に静脈内接種して、本ウイルスが鶏に対して高い病原性を示すHPAIVであることを確認しました。
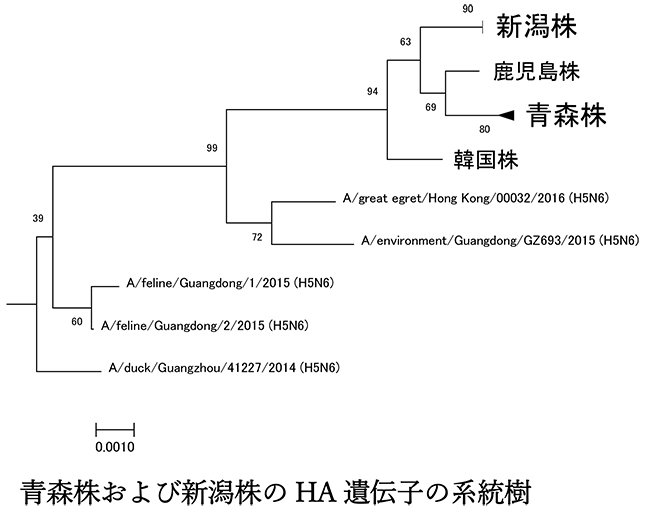
- 青森株、新潟株の由来を推定する為に、次世代シークエンサーを用いてそれぞれの全ウイルスゲノムの99.5%(青森株)および100%(新潟株)を解読しました。インフルエンザウイルスのゲノムは分節と呼ばれる8本のRNAからなり、それぞれの遺伝子がコードする主要なタンパク質により、HA, NA, PB1, PB2, PA, NP, M, NS遺伝子と呼ばれています。青森株と新潟株の8本すべての遺伝子分節は、相互に99.2%以上の相同性を示し、さらに鹿児島大学が2016年11月に鹿児島県出水市のナベヅルのねぐらの水から分離したH5N6亜型HPAIV(鹿児島株)の遺伝子とも99.3%以上の相同性を持つことが明らかとなりました。また、2016年10月に韓国で分離されたH5N6亜型HPAIV(韓国株)とも97.4%以上の相同性を持つことが確認されました。さらに、青森株、新潟株の8本の遺伝子分節のうち7本は中国広東省で2015年に流行していたH5N6亜型ウイルスと、1本は中国広東省のその他のAIVとそれぞれ97%以上の相同性を示しました。このことから、青森株と新潟株はともにナベヅルのねぐらの水から分離された鹿児島株と同一の由来であり、これらのウイルスの共通の祖先は、中国のH5N6亜型HPAIVとその他のAIVの間で起こった遺伝子再集合によって出現したウイルスであると考えられました。
- 青森株および新潟株のHA遺伝子配列から推定されるアミノ酸配列には、HPAIVに特徴的な塩基性アミノ酸が連続する配列が存在していました。インフルエンザウイルスが細胞に感染する際には、HAタンパク質が細胞表面の受容体に吸着しますが、鳥類とほ乳類では受容体が異なることが知られています。青森株、新潟株のHAタンパク質の宿主細胞への吸着に関与するアミノ酸残基は、鳥型受容体に特異性を示す配列でした。その他のウイルスタンパク質のアミノ酸配列においても、ほ乳類や人への感染性を獲得するようなアミノ酸置換は認められませんでした。また、M2タンパク質の推定アミノ酸配列から、抗ウイルス剤の一種であるアダマンタン誘導体(アマンタジン、リマンタジン)に感受性を示すことが示唆されました。NAタンパク質にはノイラミニダーゼ阻害剤耐性に関与するアミノ酸置換は認められませんでした。これらの推定アミノ酸配列に基づく解析からは、このウイルスが直接、人に感染する可能性は低いと推定されました。
今後の予定・期待
解読したゲノム配列は、近日中に公共遺伝子データベースで公開する予定です。
自然感染経路での鶏やあひるにおけるウイルスの体内動態や家禽間での伝播性、宿主の反応などをBSL-3ag施設を活用した感染実験等でより詳しく明らかにしていく予定です。
ゲノム情報から推定されたウイルスの性状について、哺乳類を用いた感染実験やウイルスの受容体特異性の解析等の技術を持った国内研究機関との連携によって、実態が明らかにされることが期待されます。
用語の解説
1)高病原性鳥インフルエンザ(HPAI)
高病原性鳥インフルエンザウイルスによって引き起こされる鶏における高い致死率が特徴の家禽の疾病。
2)(A型インフルエンザウイルスの)亜型
ウイルス表面に存在する2つの糖タンパク質(赤血球凝集素タンパク:HA、ノイラミニダーゼ:NA)の種類によるウイルス分類法。HAには、H1からH16、NAにはN1からN9までの亜型が存在する(近年コウモリから新しい亜型のウイルスが報告され、それぞれH17N10, H18N11亜型と提唱されている)。通常それぞれの種類によって、H1N1、H3N2、H5N1等と記載。
3)遺伝子再集合
インフルエンザウイルスは、そのゲノム分子として8本のRNA分節を持っている為、由来の異なる2つのインフルエンザウイルスが、同一の細胞に感染した場合、細胞質内でそれぞれのウイルスのゲノムの混合が起こることによって、新たなゲノム分子の組み合わせのウイルスが生じる現象。
4)高病原性鳥インフルエンザウイルス(HPAIV)
国際獣疫事務局(OIE)の規定による検査法によって鶏に高い致死率を示すA型インフルエンザウイルス。H5及びH7亜型の一部のウイルスが主。
5)次世代シークエンサー
従来型のサンガー法に基づくシークエンサーとは異なる技術によるシークエンスを行なう。サンガー法では、鋳型となる遺伝子に相補的なプライマーDNAが必要であったが、次世代シークエンサーでは鋳型遺伝子配列に依存せず、大量の配列が解析できるため、ゲノム配列等の解析に適している。
6)分節
ウイルスゲノムが複数の断片に分かれている場合に、それぞれの断片を分節という。主にRNAウイルスゲノムで用いられる。
7)BSL-3ag
畜産上の重要感染症病原体を取り扱う為に高度封じ込めが講じられている実験施設。Bio-safety level-3 agricultureの略。農研機構動物衛生部門ではOIEおよびWHOラボラトリー・バイオセイフティー基準適合の動物衛生高度研究施設を所有している。
参考図