開発の社会的背景
死亡羽数の増加など、家畜伝染病である高病原性鳥インフルエンザ(HPAI)または低病原性鳥インフルエンザ(LPAI)を疑う家きんの異状が認められた場合には、国が定める「高病原性鳥インフルエンザ及び低病原性鳥インフルエンザに関する特定家畜伝染病防疫指針」に従って検査が進められます。簡易検査キットを用いた抗原検査(簡易検査)によりA型インフルエンザウイルス陽性(家きんでは鳥インフルエンザウイルス)と判定された場合は、都道府県の家畜保健衛生所において当該ウイルスのHA亜型がH5またはH7であるかを判定するための遺伝子検査が行われます。その結果、いずれかの亜型であると判明し、農林水産省によってHPAIまたはLPAIと判断された場合には、まん延を防止するために殺処分を含む防疫措置が講じられます6)(図2)。そのため、ウイルス亜型を判定する遺伝子検査には、正確性と迅速性が要求される一方で、多数の検体を扱う場合には手技の煩雑化や検査結果判明までに時間を要するなど検査者の負担が大きくなっています。近年における世界的なHPAIの流行を背景にわが国へのHPAIウイルスの侵入リスクは非常に高まっており、渡り鳥が飛来する秋から春先までは特にHPAIを警戒し、家きんの検査件数が増加するなど、検査者の負担が大きくなることから、遺伝子検査法の迅速化や省力化が望まれます。
研究の経緯
HPAIウイルスは鶏に対する病原性が極めて高いことから、農林水産省、都道府県の家畜保健衛生所そして農研機構の3者が協力し、リアルタイム及びコンベンショナルRT-PCR法7)を併用した遺伝子検査体制が構築されています。農研機構とタカラバイオ株式会社は、これまでに豚熱、アフリカ豚熱、牛呼吸器病ウイルスに対する簡便かつ迅速な遺伝子検査法を共同で開発してきましたが、今回の共同研究では、鳥インフルエンザウイルスの検出とHA亜型の決定に現在使用しているリアルタイムRT-PCR法を改良し、迅速かつ省力的な遺伝子検査を可能にするマルチプレックスリアルタイムRT-PCR法の開発を試みました。
研究の内容・意義
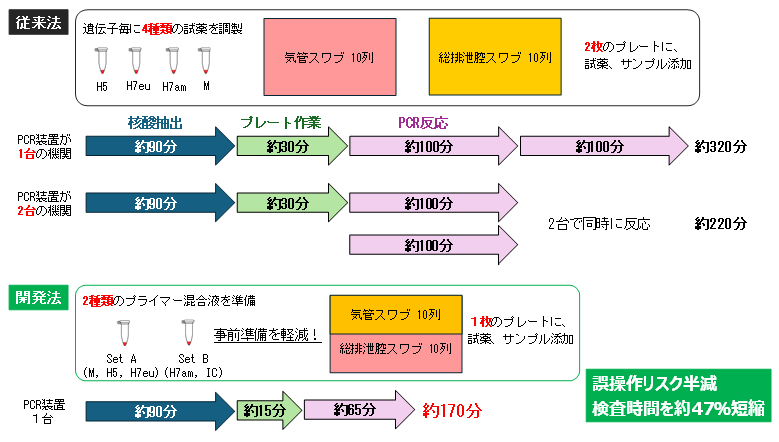
- 現行の遺伝子検査法(図1上段、従来法)
特定家畜伝染病防疫指針に基づく検査では、異状が確認された農場において死亡家きん(8羽)と生存家きん(2羽)の気管および総排泄腔スワブ(10羽×2種類のスワブ=20検体)を採取後、核酸を抽出し、鳥インフルエンザウイルス(M遺伝子)の検出とHA亜型(H5かH7か)の決定を目的としたリアルタイムRT-PCRを実施します。現行のリアルタイムRT-PCR法では、M、H5及び2系統のH7遺伝子(H7eu:ユーラシア型とH7am:アメリカ型)の4種類を個別に検出するため、20検体の検査には96ウェルプレートを2枚使用しなければなりません。このため、PCR装置を1台しか保有しない機関では検査に約320分程度の時間が必要でした。PCR装置を2台保有している機関では2枚のプレートを一度に処理できますが、それでも約220分程度の時間がかかります。
- 新たな遺伝子検査法(図1下段、開発法)
今回、M遺伝子を検出するプライマー&プローブ、H5遺伝子を検出するプライマー&プローブおよびH7eu遺伝子を検出するプライマー&プローブの3種類を組み合わせて混合したSet AとH7am遺伝子に対するプライマー&プローブおよびインターナルコントロール8)を組み合わせて混合したSet Bの2種類の試薬を作製しました。今回の共同研究で開発したマルチプレックスリアルタイムRT-PCR法では、各検体に対してSet A及びSet Bの試薬をそれぞれ反応させることで、96ウェルプレート1枚を使い、全ての検体についてA型インフルエンザウイルスの検出とHA亜型の決定を行うことが可能になります。プレート操作が半減することに加え、新たな方法ではRT-PCRの反応時間自体も短縮できたことから、PCR装置を1台しか保有しない機関でも約170分で検査が終了し、検査時間を最大で47%削減できます。
- 検査法の特異性と検出感度
今回、タカラバイオ株式会社は同社が保有する遺伝子増幅技術を農研機構に提供し、農研機構と共同で検査法の開発に取り組むとともに、農研機構は、保有する様々なHA亜型の鳥インフルエンザウイルスを用いて当該検査法の特異性と検出感度の実証を行いました。その結果、本検査法は、現行の遺伝子検査法と同等の特異性と検出感度を示すことが確認されました。
新たな検査法では、現行の遺伝子検査法に比べ、検査者の操作が半減し、誤操作のリスクや判定に要する時間が大幅に削減されます。
今後の予定・期待
共同開発した検査法は、国が定める「高病原性鳥インフルエンザ及び低病原性鳥インフルエンザに関する特定家畜伝染病防疫指針」を踏まえて定められる「高病原性鳥インフルエンザ及び低病原性鳥インフルエンザに関する特定家畜伝染病防疫指針に基づく遺伝子検査の方法について」(令和6年9月30日付け6消安第3679号)に則った遺伝子検査法の一つとして国や都道府県の病性鑑定施設等において利用されることが期待されます。また、この成果は検査の迅速化や省力化への貢献が期待されます。
用語の解説
- 高病原性鳥インフルエンザ(HPAI)ウイルス
-
鶏に高い致死率を示すA型鳥インフルエンザウイルスで、国際獣疫事務局(WOAH)の規定に従い、分離ウイルスの鶏への静脈内接種試験やHAタンパク質の開裂部位における連続した塩基性アミノ酸配列の存在によって判定されます。
[ポイントへ戻る]
- マルチプレックスリアルタイムRT-PCR法
-
増幅したい遺伝子(標的遺伝子)をはさむように一組の短いDNA鎖(プライマー)を設計し、これを起点にして耐熱性のDNA合成酵素を反復して作用させることにより標的遺伝子を合成、増幅する方法をPCR(polymerase chain reaction)法といいます。このうち、特に標的遺伝子の増幅過程を専用の検出機器でリアルタイムに検出し、解析するRT-PCR法をリアルタイムRT-PCR法と呼びます。また、検出方法として、様々な色の蛍光標識を付加したプローブと呼ばれる短い核酸を組み合わせることで、複数の標的遺伝子を同時に識別しながら検出することが可能となります。このような検出方法をマルチプレックスリアルタイムRT-PCR法と呼びます。
[ポイントへ戻る]
- 高病原性鳥インフルエンザ(HPAI)
-
高病原性鳥インフルエンザウイルスによって引き起こされ、鶏に高い致死率を示す家きんの疾病で、野鳥にも感染します。家畜伝染病予防法により家畜伝染病に指定されています(https://www.maff.go.jp/j/syouan/douei/tori/attach/pdf/index-49.pdf)。
[概要へ戻る]
- (A型インフルエンザウイルスの)亜型
-
インフルエンザウイルスの表面に存在する2つの糖タンパク質(ヘマグルチニン:HA,ノイラミニダーゼ:NA)の種類に基づくウイルスの分類を指します。鳥インフルエンザウイルスのHAにはH1からH16まで、NAにはN1からN9までの亜型が存在し、それぞれの亜型を組み合わせてH1N1、H3N2、H5N1等と記載されます。
[概要へ戻る]
- 96ウェルプレート
-
PCR反応用の実験器具で、96ウェルが縦8列、横12列で並んでいるプレート。
[図1へ戻る]
- 亜型による防疫措置の要否
-
高病原性鳥インフルエンザ(HPAI)の原因ウイルスはH5またはH7亜型の鳥インフルエンザウイルスです。H5またはH7亜型のウイルスには低病原性のウイルスもありますが、ほとんど臨床症状を示さずに家きんの中で維持されることによって、原因ウイルスがHPAIウイルスに変異した事例が確認されていることから、H5またはH7亜型の場合は防疫対象となります。
[開発の社会的背景へ戻る]
- コンベンショナルRT-PCR法
-
リアルタイムPCR法とは異なり、PCR反応後に電気泳動によって標的遺伝子の増幅の有無を確認する従来の手法をコンベンショナルPCR法と呼びますが、鋳型がRNAである場合にはPCR反応前に逆転写(Reverse Transcription: RT)反応を行いRNAからDNAに変換する必要があるため、コンベンショナルRT-PCRと呼ばれています。
[研究の経緯へ戻る]
- インターナルコントロール(IC)
-
カラム精製等の簡易核酸抽出法により調製した試料を用いたPCRによって陰性の結果を得た場合は、反応阻害の影響によるものではないことを確認する必要があります。PCR阻害を受けやすい低濃度の鋳型DNA(インターナルコントロール)を反応系に添加し、シグナル増幅を確認することにより、PCR阻害による偽陰性の可能性を排除し、得られた結果の信頼性が担保されます。
[研究の内容・意義へ戻る]
参考図
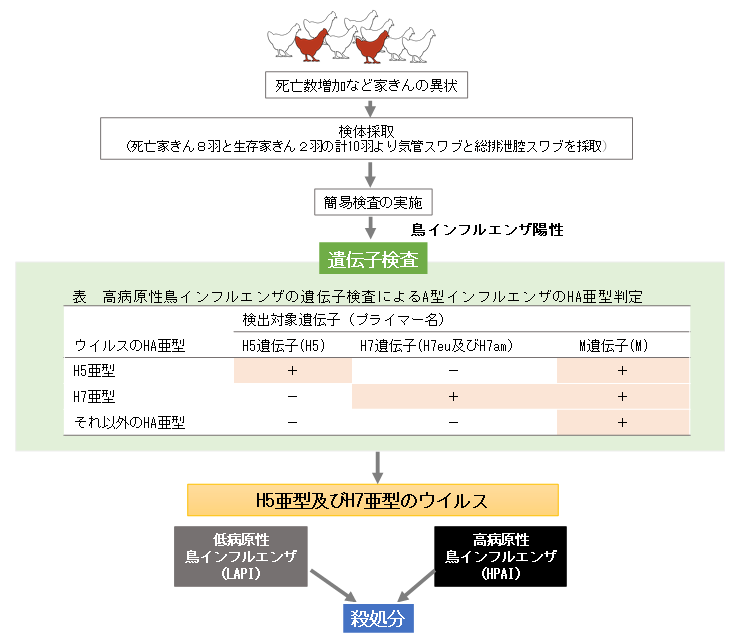
図2. 鳥インフルエンザの防疫措置の流れ
家きんの異状が認められた農場において簡易検査によりA型インフルエンザウイルスが検出された場合は遺伝子検査を実施する。検査対象のウイルスがH5またはH7亜型と判定された場合は防疫措置の対象となる。