ポイント
- 2024年シーズンに国内の家きんより分離1)された高病原性鳥インフルエンザウイルス2)について、11事例目までのウイルスゲノムを解析し、遺伝子型を決定しました。
- 遺伝子型は4種類に分類され、4シーズン連続して検出されている1種類の遺伝子型に加え、新たに3種類の遺伝子型が含まれました。
- シーズン初期の6週間で4種類の遺伝子型のウイルスが家きんに侵入していることから、引き続き家きん飼養施設へのウイルス侵入に対する警戒が必要です。
概要
2024年シーズンは、10月17日に家きんでシーズン初となる高病原性鳥インフルエンザ(HPAI)の発生が報告され、2025年1月22日までに家きん飼養施設で計42件発生しています。
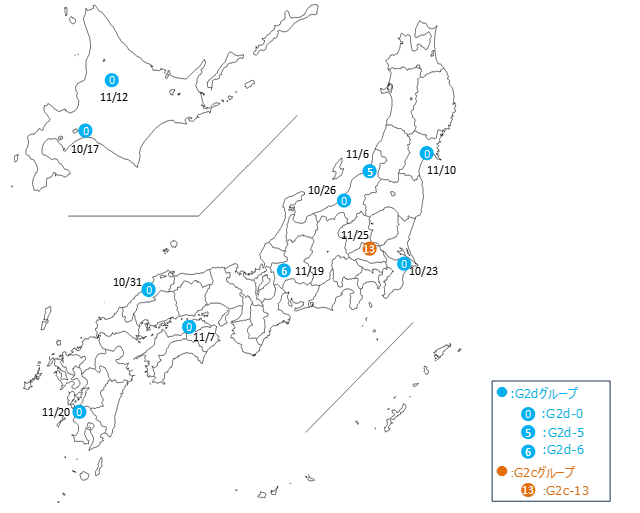
農研機構は、2024年10月の初発から11月末までの6週間に家きんで発生した11事例から分離されたH5N1亜型3)HPAIウイルス計11株の全ゲノム解析を行い、4種類の遺伝子型(G2d-0:8株、G2d-5、G2d-6及びG2c-13:各1株)に分類されることを明らかにしました。遺伝子型G2d-0は2021年シーズン以降、国内で4シーズン連続して検出されています。また、家きんの2024年シーズン初発に先立って9月30日に北海道の野鳥から検出されたウイルスも同型でした。これらのウイルスは2024年シーズンに渡り鳥によって運ばれてきたと推測されます。その他3種類の遺伝子型は、2024年シーズンに新たに同定された遺伝子型で、一部の遺伝子分節4)が国内外の野鳥で検出された鳥インフルエンザウイルスやHPAIウイルスに由来していました。これは、カモなどの野鳥集団で感染を繰り返すことで、HPAIウイルスに遺伝子再集合5)が起こった結果、新たに出現したと考えられます。
また、2024年シーズンに分離された遺伝子型G2d-0の代表ウイルス株について、鶏の自然感染経路である経鼻接種による感染実験を行ったところ、高い致死性を示し、病原性はこれまでのシーズンに分離された同型株と明確な差異は認められませんでした。
なお、2024年シーズン11月までに分離されたウイルス株の推定アミノ酸配列解析の結果、代表的な抗ウイルス薬への耐性及び哺乳類でのウイルス増殖に関連する変異は見つかっておらず、これらのウイルス株が直ちにヒトでの流行を引き起こすリスクは低いと考えられます。
秋に国内で越冬する渡り鳥により持ち込まれたウイルスは、渡り鳥の間で春先に繁殖地へ北帰するまで保持され、渡り鳥の移動にともないウイルスも国内の各地に移動すると推察されます。このような状況を踏まえ、発生の低減に向けて、国内家きん飼養施設へのウイルス侵入防止対策の徹底と疾病の早期発見に一層努める必要があります。
関連情報
予算 : 農林水産省委託研究「安全な農畜水産物安定供給のための包括的レギュラトリーサイエンス研究推進委託事業」のうち、「新たな感染症の出現に対してレジリエントな畜産業を実現するための家畜感染症対策技術の開発」(JPJ008617.23812859)

